L’Agenzia Italiana del Farmaco (AIFA) fornisce sul suo sito settimanalmente aggiornamenti relativi al trattamento con i nuovi farmaci ad azione antivirale diretta di seconda generazione (DAAs) per la cura dell’epatite C cronica (per approfondire si rimanda all’intervista con il prof. Colombo in homepage), raccolti dai Registri di monitoraggio appositamente istituiti.
Nuove strategie garantirebbero a tutti il trattamento dell’epatite C
Come è noto, i costi del trattamento per l’epatite C, dimostratisi altamente efficaci, sono notevoli, soprattutto tenendo conto del numero elevato di pazienti affetti da epatite C cronica. Con l’obiettivo finale di favorire l’accesso al nuovo trattamento nonché ai farmaci e alle terapie per l‘epatite C a tutti i pazienti, garantendo al tempo stesso la sostenibilità per il Sistema Sanitario Nazionale, si è reso necessario individuare una strategia di accesso graduale dei pazienti, sulla base dell’urgenza clinica al trattamento.
I criteri clinici secondo l’AIFA per il trattamento dell’epatite C
A seguito di un lungo lavoro di un Tavolo tecnico epatite C istituito presso l’Agenzia, la Commissione Tecnico Scientifica (CTS) dell’AIFA ha individuato una serie di criteri clinici che rappresentano le priorità per la rimborsabilità del trattamento con i nuovi farmaci contro l’epatite C (DAAs), vale a dire:
- Pazienti con cirrosi in classe di Child A o B e/o con HCC con risposta completa a trattamento resettivo, chirurgico o loco-regionale non candidabili a trapianto epatico nei quali l’eptite C sia determinante per la prognosi.
- Epatite ricorrente HCV-RNA positiva del fegato trapiantato in paziente stabile clinicamente e con livelli ottimali di immunosoppressione.
- Epatite cronica con gravi manifestazioni extra-epatiche HCV-correlate (sindrome crioglobulinemica con danno d’organo, sindromi linfoproliferative a cellule B).
- Epatite cronica con fibrosi METAVIR F3 (o corrispondente Ishack).
- In lista per trapianto di fegato con cirrosi MELD <25 e/o con HCC all’interno dei criteri di Milano con la possibilità di una attesa in lista di almeno 2 mesi.
- Epatite cronica dopo trapianto di organo solido (non fegato) o di midollo con fibrosi METAVIR ≥2 (o corrispondente Ishack).
- Epatite cronica con fibrosi METAVIR F0-F2 (o corrispondente Ishack) (solo per simeprevir).
L’obiettivo iniziale era di garantire, con i fondi disponibili, il trattamento dell’epatite C di almeno 50.000 pazienti. Secondo i dati dei Registri AIFA, questo numero è stato superato nel giugno scorso, incrementando linearmente dal febbraio 2015. All’aggiornamento pubblicato il 18 luglio, i trattamenti per l’epatite C intrapresi in Italia sono oltre 51.000 (Figura).
Monitoraggio AIFA sul trattamento per l’epatite C
In relazione alla priorità di selezione dei pazienti, il criterio 1 risulta quello di gran lunga più frequentemente riportato, in circa 2/3 dei casi (oltre 34.000), seguito dal criterio 4 (circa 12.000 casi, 23%) e, con frequenza nettamente inferiore, dai criteri 3 e 2 (circa 2200 e 1600 casi, rispettivamente). I criteri 7, 5 e 6 sono stati applicati in poche centinaia di pazienti.
Questo monitoraggio appare di grande utilità per definire le esigenze cliniche dei pazienti con epatite cronica C e consentirà di verificare anche l’efficacia del trattamento innovativo dell’epatite C, secondo il profilo clinico di indicazione. L’AIFA è inoltre impegnata in una continua e tempestiva verifica delle nuove evidenze scientifiche, in modo da rimodulare i vigenti criteri di eleggibilità al trattamento con i nuovi farmaci contro l’epatite C (DAAs) e garantire il più ampio accesso possibile a questi farmaci altamente efficaci.
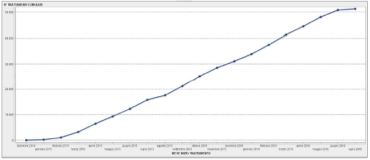
Figura: Andamento nel tempo del numero di trattamenti con i nuovi farmaci antivirali diretti anti-epatite C